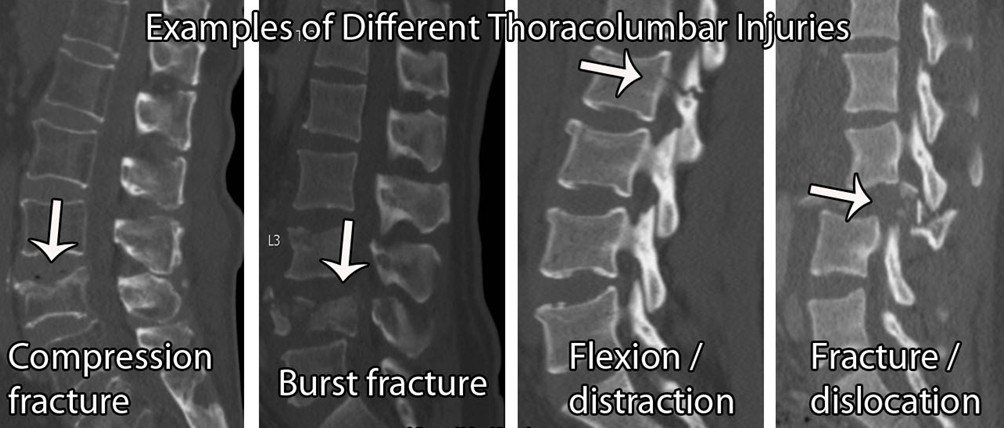
Bandiere rosse spinali
Per troppo tempo i fisioterapisti hanno posto le stesse domande standard per effettuare uno screening medico del paziente. "Ha problemi al petto o al cuore, diabete, epilessia o problemi circolatori?" è un esempio comune e spesso è clinicamente irrilevante. Negli ultimi anni la compressione del midollo spinale è passata dal radar dei chirurghi ortopedici a quello dei fisioterapisti e quindi domande come "ha problemi intestinali o vescicali?" sono state incluse nei nostri esami soggettivi. Tuttavia, questo non è ancora abbastanza dettagliato, perché, ad esempio, un paziente potrebbe non considerare un sintomo di una grave patologia come un "problema", se è diventato la sua normalità.
Mi scuso per l'inizio provocatorio, ma nei miei 34 anni di esperienza clinica ho visto troppo spesso questa domanda standardizzata.
L'interrogatorio di un paziente sulle bandiere rosse è soggetto al ragionamento clinico, come tutte le nostre domande. Pertanto, le domande sulle bandiere rosse devono essere personalizzate per ogni individuo e devono inseguire l'ipotesi appropriata che si sviluppa nella mente del fisioterapista, a partire dalle informazioni raccolte da ogni singolo paziente. Tuttavia, sviluppare un'ipotesi medica appropriata può essere la nostra prima sfida, perché in medicina (e in fisioterapia) "si vede solo ciò che si cerca e si riconosce solo ciò che si sa già". Questo viene spesso definito "pregiudizio di conferma" e si basa sul fatto che "vediamo ciò che vogliamo vedere", perché solo così possiamo credere di poter aiutare il paziente (dobbiamo sapere cosa stiamo trattando per sapere come trattarlo). Ecco perché è importante ampliare il più possibile le nostre conoscenze mediche, per evitare che ci sfugga qualcosa che non conosciamo!
Questo vale anche per alcune delle diagnosi più ovvie, per non parlare di quelle più complesse e rare. Ad esempio, fino a 70% di fratture vertebrali sono diagnosticate in modo errato e fino a 75% di infezioni spinali sono inizialmente diagnosticate in modo errato (Grigoryan et al 2003, McCarthy & Davis 2016). L'infezione spinale è difficile da riconoscere clinicamente. Nei pazienti che ho visto con infezione spinale, sapevo che c'era qualcosa di molto sbagliato nel paziente, ma non sapevo esattamente cosa, e solo indagini appropriate hanno scoperto la diagnosi. Anche questo fa parte del nostro ruolo nello screening: dobbiamo sapere quando sono necessarie ulteriori indagini e quali potrebbero essere utili.
Se consideriamo la differenza tra la diagnosi medica e la diagnosi fisioterapica, la prima cerca di trovare la causa del problema del paziente, mentre il fisioterapista ne cura le conseguenze. La determinazione delle conseguenze si basa principalmente sui risultati clinici, mentre la determinazione della causa della sofferenza del paziente si basa in gran parte su conoscenze teoriche e rientra quindi nel campo del modello biomedico. Quindi, come fisioterapisti dovremmo lavorare principalmente secondo il modello biopsico-sociale, ma dobbiamo comunque considerare il modello bio-medico nel nostro ruolo di screening medico.
In poche parole, l'approccio biomedico può essere utilizzato per esaminare il paziente alla ricerca di "red flags" e di condizioni che richiedono un'attenzione medica precoce, mentre l'approccio biopsicosociale deve essere preso in considerazione per capire come il problema stia colpendo il paziente, concentrandosi sui segni e sui sintomi piuttosto che sulla diagnosi strutturale. Come si può vedere nel diagramma seguente, lo screening dei segnali di allarme dovrebbe essere una componente prioritaria del processo di visita di tutti i nostri pazienti.
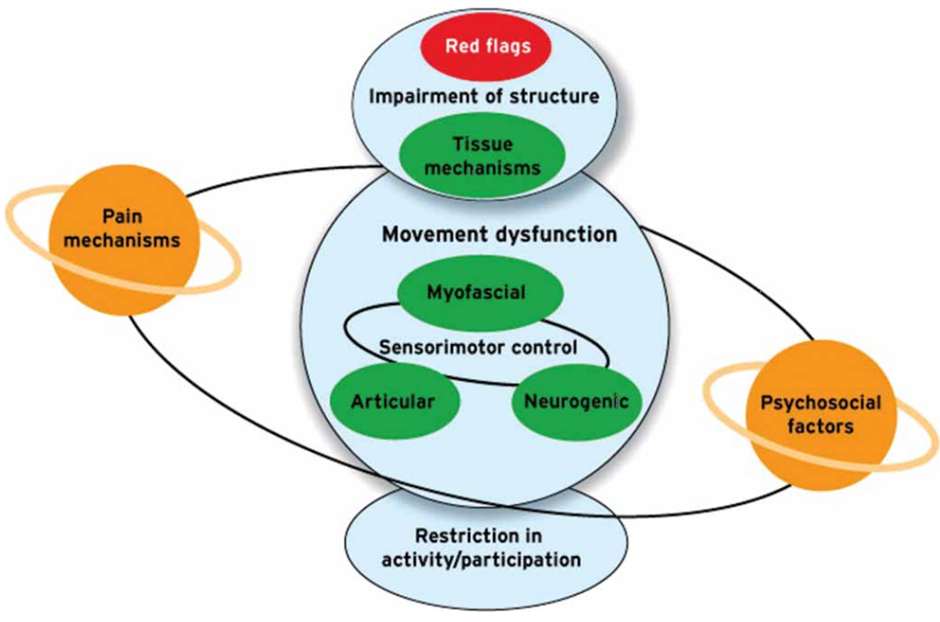
Va riconosciuta la nostra difficoltà a stabilire una diagnosi medica dei pazienti con LBP, ad esempio, ma nonostante ciò il modello biomedico ha ancora un ruolo nel guidare le decisioni relative alla gestione dei pazienti, allo screening medico e alla prognosi. Quando si considera la diagnosi medica, il paziente viene effettivamente sottoposto a un triage medico e di solito ciò può essere fatto attraverso un'anamnesi dettagliata supportata da esami medici (esami del sangue, scansioni, ecc.) piuttosto che sulla base dei risultati di qualsiasi test fisico.
Non è saggio dare per scontato che se il paziente ha visto un medico prima del vostro appuntamento, sia già stato sottoposto a uno screening medico. I medici di solito hanno un tempo molto limitato per i loro pazienti e ho molti esempi di pazienti con patologie gravi che hanno già visto il loro medico di base. Inoltre, come fisioterapisti pensiamo in modo molto muscoloscheletrico e di conseguenza siamo tentati di credere che ogni paziente che vediamo abbia un problema muscoloscheletrico. Quindi, sia che si lavori come operatore di primo contatto (nel settore pubblico in alcuni paesi e/o nel settore privato nella maggior parte dei paesi) sia che si lavori come operatore secondario, è necessario effettuare uno screening a bandiera rossa basato sulle conoscenze mediche per assicurarsi di non trattare un paziente che dovrebbe essere curato altrove. "Vedere la persona giusta, al momento giusto, per il trattamento giusto" (European Parliament Health Briefing 2015).
Le bandiere rosse sono possibili indicatori di patologie gravi, segnali di allarme che la Fisioterapia può non o guide di previsione clinica. Dovrebbero rappresentare una chiara ragione per ulteriori indagini o per un successivo invio medico.

Dopo tutto, non è nell'interesse di nessuno trattare un lupo travestito da pecora!
Le linee guida cliniche per la gestione fisioterapica dei LBP persistenti (CSP, 2007) riportano che ci sono 163 voci individuali che potrebbero essere considerate bandiere rosse per la patologia spinale, 119 voci nell'anamnesi soggettiva e 44 voci nell'esame fisico. È chiaro che questo rappresenta un problema per l'utilità clinica pratica delle bandierine rosse. Inoltre, mancano prove valide a sostegno dell'efficacia informativa della maggior parte delle bandierine rosse. Henschke et al. (2013) hanno riferito che le bandierine rosse in combinazione sono promettenti, ma sono necessari ulteriori studi di validazione.
Tuttavia, le bandierine rosse sono ancora considerate l'indicatore clinico più affidabile di una potenziale patologia grave e rimangono fondamentali per il nostro processo di valutazione (Underwood, 2013). Poiché la gravità di alcune bandierine rosse giustifica un'azione immediata, mentre altre giustificano solo un'osservazione conservativa, è importante classificare ogni reperto e rispondere in base al livello di gravità del reperto stesso. Alcune bandiere sono più rosse di altre!
Sizer et al. (2007) hanno classificato le bandiere rosse in 3 gruppi:
- Categoria I
- Fattori che richiedono un'attenzione medica immediata
- Categoria II
- Fattori che richiedono un'interrogazione soggettiva e procedure di esame e trattamento precauzionali
- Categoria III
- Fattori che richiedono ulteriori test fisici e analisi di differenziazione
Qualsiasi segnale di allarme della categoria I può suggerire una patologia grave. Questi includono deficit neurologici non spiegati da una monoradicolopatia, alterazioni sensoriali della regione perianale, alterazioni patologiche dell'intestino e della vescica, andamento non meccanico dei sintomi, deficit neurologico progressivo e masse addominali pulsanti.
I campanelli d'allarme di categoria II includono età di insorgenza > 50 anni, clono, febbre, esami ematici infiammatori elevati (VES), deficit dell'andatura, anamnesi di un disturbo con predilezione per le infezioni o le emorragie, o di un disturbo metabolico delle ossa, o di un cancro, uso di corticosteroidi a lungo termine, piaghe o ferite che non guariscono e un'anamnesi recente di perdita di peso inspiegabile.
Una singola bandierina rossa di categoria II potrebbe non destare preoccupazione, ma più bandierine rosse si identificano in un paziente, più l'indice di sospetto deve aumentare. È necessario prendere in considerazione anche alcuni gruppi di segnali di allarme; un paziente con LBP con un'età di insorgenza superiore ai 50 anni e che assume steroidi a lungo termine ha una probabilità molto maggiore di subire una frattura da compressione spinale. Secondo Jarvik et al. (2002) un paziente con fallimento di un precedente trattamento conservativo + perdita di peso inspiegabile + storia di cancro + età superiore ai 50 anni = una sensibilità di quasi 100% per l'identificazione di una neoplasia.
I segnali di allarme di categoria III comprendono riflessi anomali, radicolopatia o parestesia bilaterale o unilaterale, dolore riferito inspiegabile e debolezza significativa inspiegabile degli arti superiori o inferiori.
Inoltre, esistono segnali di allarme non specifici, come una presentazione clinica diversa dai modelli clinici noti, nessuna risposta al trattamento (migliore o peggiore) e un comportamento dei sintomi nel tempo che non corrisponde alla prognosi. Uno qualsiasi di questi eventi clinici dovrebbe indurre a pensare a una possibile condizione non meccanica, che potrebbe richiedere ulteriori indagini e/o interventi medici.
Per quanto riguarda le eziologie spinali gravi, le più comuni da considerare sono la sindrome della cauda equina, le fratture, le lesioni benigne o maligne e le infezioni. Il riconoscimento precoce di una patologia grave dipende dalla consapevolezza, dalla vigilanza e dal sospetto piuttosto che dalle regole (Grieve, 1994). La consapevolezza deriva dall'aumento delle nostre conoscenze mediche e la vigilanza è legata al dettaglio delle domande e dell'esame di ogni paziente. Poiché la maggior parte dei segnali di allarme si trova nell'esame soggettivo, è essenziale interrogare attentamente ogni paziente.
Sindrome della cauda equina (CES):

Purtroppo non esistono criteri diagnostici definitivi ampiamente accettati per la CES. Fraser et al. (2009) hanno identificato 17 definizioni diverse! La sfida diagnostica è ulteriormente aggravata dal fatto che i segni e i sintomi iniziali sono spesso sottili e vaghi e variano in intensità e progressione. Solo grazie a un'anamnesi attenta e dettagliata e all'esame del paziente, la CES può essere diagnosticata precocemente e quindi trattata tempestivamente per evitare disabilità a vita (Ma et al, 2009).
Di tutte le bandiere rosse elencate in relazione al CES, vi sono ci sono 5 caratteristiche chiave che sono costantemente descritte in letteratura e che quindi dovrebbero costituire la base delle vostre domande relative alla diagnosi. Si tratta di sciatica neurogena bilaterale, ridotta sensazione perineale, ritenzione vescicale indolore, perdita del tono anale e perdita della funzione sessuale. Il livello di evidenza per tutti questi segni e sintomi, da soli, è BASSO. Quindi, ancora una volta, è necessario affidarsi al giudizio clinico e considerare l'intero quadro, e più i risultati sono significativi, più l'indice di sospetto dovrebbe aumentare. L'anamnesi e la tempistica sono importanti. Se tutti i cambiamenti sono recenti, potrebbe essere necessario un intervento urgente.
Greenhalgh et al. nel 2018 hanno consigliato di approfondire le domande sull'intestino e sulla vescica per contribuire allo screening della CES. Hanno consigliato 3 importanti domande di screening:
Domanda vitale 1: Ha notato intorpidimento o strane sensazioni intorno alle natiche o tra le gambe? La carta igienica è normale quando si pulisce il sedere?
Domanda vitale 2: La vescica funziona normalmente? Riesce a capire quando è piena? Ha avuto perdite di controllo (incidenti) o difficoltà a urinare? Oppure ha avuto la sensazione di volerla fare sempre?
Domanda vitale 3: Ha avuto di recente problemi insoliti con l'intestino? Ha notato cambiamenti nella funzione sessuale, come una perdita di sensibilità nei genitali o l'impossibilità di avere un'erezione o di eiaculare?
Se si sospetta una CES, tutta la letteratura concorda sulla necessità di un parere medico e di un intervento urgente, per cui è appropriato un invio al pronto soccorso. È essenziale una decompressione chirurgica precoce, che ha un'ampia letteratura a sostegno, ma c'è controversia sui tempi: molti autori sostengono che l'intervento chirurgico sia ottimale entro 48 ore (dalla comparsa di disfunzioni intestinali o urinarie) per un buon recupero. Pertanto, anche se la diagnosi precoce è difficile, se si hanno dei sospetti è meglio essere sicuri che dispiaciuti e rivolgersi al più presto. "Non si guadagna nulla ritardando l'intervento e si può perdere molto" (Germon et al, 2015).
Frattura spinale:
In generale, le bandiere rosse per la diagnosi di fratture vertebrali non sono utili. Ci sono molti falsi positivi, con una bassa accuratezza diagnostica (Williams et al 2013). Pertanto, se si sospetta una frattura, è importante interrogare il paziente sui fattori di rischio più ampi.
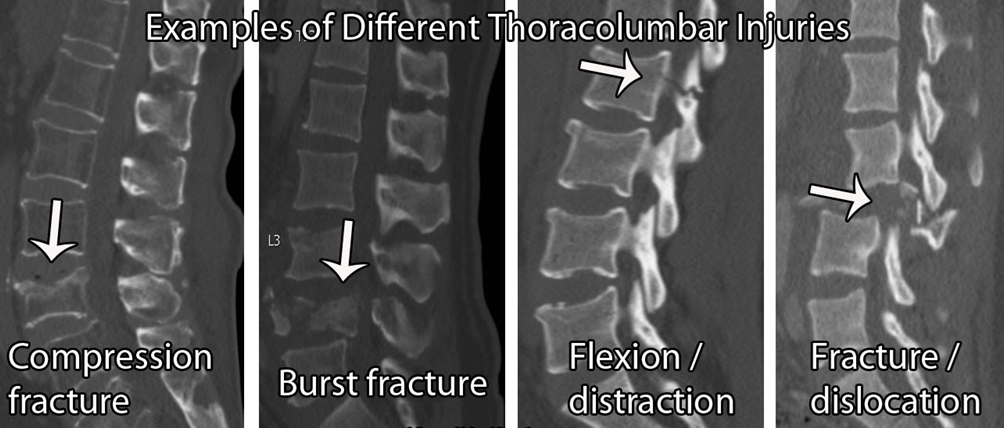
I fattori di rischio per l'indebolimento osseo includono: eccesso di alcol (≥ 3 unità al giorno), carenza di vitamina D, uso di steroidi a lungo termine. (≥5mg/die per 3 mesi), artrite reumatoide, diabete, fumo ( ≥ 20/die), restrizioni dietetiche, disturbi alimentari, problemi di assorbimento, ad esempio morbo di Crohn. Anche in questo caso, il livello di evidenza per la maggior parte di questi elementi è basso e quindi, più risultati positivi si ottengono, più si è sospettosi.
Se un paziente si presenta in ambulatorio con un'improvvisa insorgenza di dolore toracico o lombare, una frattura dovrebbe essere tra i sospetti. Questa ipotesi sarebbe ulteriormente avvalorata se il paziente avesse una storia di precedenti fratture osteoporotiche, altri fattori di rischio osteoporotico (come sopra), una storia passata di cancro, osteoporosi nota o mieloma, tenderness osseo sulla linea mediana e/o un esordio oltre i 65 anni nelle donne o oltre i 75 nei maschi.
Malignità spinale:
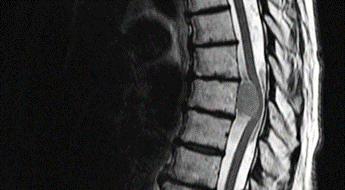
Dopo la frattura vertebrale, la malattia ossea metastatica è il 2nd la più comune patologia grave della colonna vertebrale. Le metastasi ossee spinali sono comuni per i tumori della mammella, dei bronchi/polmoni, della tiroide, dei reni e della prostata. Anche in questo caso, la cattiva notizia è che non esistono segnali di allarme specifici per le neoplasie spinali, quindi dobbiamo considerare i segnali di allarme per il cancro in generale.
Questi includono:
Dolore con sollievo minimo (costante e notturno), ma è bene tenere presente che alcuni dolori da cancro sono alleviati dai farmaci e che il dolore non è sempre una presentazione precoce,
Precedenti anamnestici di cancro,
Età di insorgenza > 50 anni, o meno di 20 anni
Stanchezza, malessere sistemico,
Perdita di peso (fino a 5-10% del peso corporeo nell'arco di 3-6 mesi, Nicholson et al 2019), ma si noti che la perdita di peso non è sempre un fattore, soprattutto nelle fasi iniziali.
Nello screening delle neoplasie nei pazienti affetti da LBP, una revisione sistematica condotta da Henschke et al. nel 2007 ha rilevato che le caratteristiche e gli esami più utili sono un'anamnesi pregressa di cancro, una VES elevata, un ematocrito ridotto e il giudizio clinico. L'unico fattore con un alto livello di evidenza è l'anamnesi precedente di tumori con una predilezione per le metastasi.
La presenza di metastasi nella colonna vertebrale può portare alla compressione metastatica del midollo spinale (MSCC). Delle 163 bandiere rosse, nessuna è specifica per l'MSCC. La sfida per noi è che è difficile da diagnosticare e la diagnosi precoce è molto importante perché i ritardi nella diagnosi e nel trattamento possono portare a paraplegia e doppia incontinenza.
Turnpenney et al. (2013) hanno stilato un elenco di segnali di allarme precoci per il MSCC, che dovremmo considerare come base per le nostre domande di allarme:
Referred back pain multi-segmental or band like,
Edolore scalare, scarsa risposta al trattamento,
Dcarattere o sede diversa rispetto ai sintomi precedenti,
Fsensazioni strane o gambe pesanti,
LL'appiattimento aumenta il dolore alla schiena,
Adolore gonfiante che provoca angoscia e disperazione,
Gdisturbi del respiro, instabilità, soprattutto sulle scale,
Sdisturbi della pipì con dolore peggiore durante la notte.
Qualsiasi combinazione di queste bandiere rosse dovrebbe aumentare i sospetti e più sono le bandiere rosse, più alto è il rischio e maggiore è l'urgenza di indirizzare il paziente all'assistenza medica.
Infezione spinale:

L'infezione spinale si riferisce a qualsiasi malattia infettiva delle strutture spinali, ad esempio le vertebre, i dischi o i tessuti paraspinali adiacenti. Anche in questo caso, purtroppo, l'infezione spinale è difficile da riconoscere clinicamente. Nei Paesi ad alto e medio reddito, il tasso di infezione è aumentato costantemente, probabilmente a causa dell'invecchiamento della popolazione e dell'aumento dell'uso di farmaci per via intravenosa. Anche nei Paesi a basso reddito è aumentato, forse a causa delle epidemie di HIV/Aids e tubercolosi (Lener et al, 2018).
Quando si prende in considerazione un'infezione spinale, è ancora una volta importante interrogare il paziente in modo appropriato, il che implica lo screening dei fattori di rischio associati (Yusuf et al, 2019).
Questi includono:
Comorbidità immunosoppressive come diabete, uso di steroidi a lungo termine, fumo, HIV/AIDS;
Fattori sociali come l'uso di droghe per via endovenosa, l'obesità e una storia familiare di tubercolosi;
Fattori ambientali come le condizioni di vita (sovraffollamento, senzatetto, carcere) e il paese di nascita (nato in un paese endemico per la TBC);
Precedente intervento chirurgico alla colonna vertebrale.
Tutte le prove di allarme rosso che indicano un'infezione spinale, singolarmente, sono di basso livello. Quindi, ancora una volta, più bandiere rosse si trovano, più il livello di sospetto deve aumentare e ci si deve affidare in qualche misura al giudizio clinico. Le domande che devono essere poste e vagliate nell'esame soggettivo sono la costanza del dolore (C/C), il dolore di elevata intensità, l'insorgenza improvvisa, la febbre, i brividi, la sudorazione, l'eruzione cutanea (Herpes zoster), l'affaticamento, il malessere, la perdita di peso inspiegabile, un intervento chirurgico o un'infezione recente (ultime 4 settimane) e il dolore notturno (>60 minuti per stabilizzarsi).
Il tempo che intercorre tra l'insorgenza di un'infezione e la diagnosi è spesso prolungato. I pazienti possono essere relativamente sani fino alla manifestazione dei sintomi nelle fasi successive. La progressione è comunemente più lineare (la progressione di una neoplasia maligna può avere un andamento altalenante). Della triade dell'infezione (dolore spinale, febbre e disfunzione neurologica), il dolore lombare è il sintomo più comune, che può evolvere in sintomi neurologici. Tuttavia, molte persone non presentano tutti e tre i sintomi, solo il 50% dei pazienti riporta la febbre (Lener et al 2018). Pertanto, l'assenza di febbre non può escludere un'infezione spinale. La progressione non trattata può portare a paralisi, instabilità spinale e morte. Pertanto, come per tutte queste condizioni, vale la pena di notare che il mancato invio di un paziente come necessario è una forma di danno per il paziente, cosa che il nostro screening delle bandierine rosse cerca di prevenire.
Conclusione:
La prevalenza di gravi patologie della colonna vertebrale è rara, e la letteratura cita da 1% (Wilk, 2004) a 14,8% (Street et al, 2020). Tuttavia, possiamo vedere rapidamente 100 pazienti con LBP e alcuni di questi potrebbero avere una causa sinistra e avere bisogno di un posto diverso dalla vostra clinica. Pertanto, i medici devono essere in grado di identificare i pazienti che necessitano di un intervento medico e la migliore possibilità di raggiungere questo obiettivo è rappresentata da domande appropriate, clinicamente motivate e dettagliate.
Buona fortuna e auguri,
Matteo

Riferimenti:
Finucane, L. M., Downie, A., Mercer, C., Greenhalgh, S. M., Boissonnault, W. G., Pool-Goudzwaard, A. L., Beneciuk, J. M., Leech, R. L., & Selfe, J. (2020). Quadro internazionale per le bandiere rosse per le potenziali patologie spinali gravi. Giornale di Terapia Fisica Ortopedica e Sportiva, 50(7), 1-23. https://doi.org/10.2519/jospt.2020.9971
Fraser, S., Roberts, L. e Murphy, E. (2009). Sindrome della cauda equina: A Literature Review of Its Definition and Clinical Presentation. Archivi di Medicina Fisica e Riabilitazione, 90(11), 1964-1968. https://doi.org/10.1016/j.apmr.2009.03.021
Germon, T., Ahuja, S., Casey, A. T. H., Todd, N. V., & Rai, A. (2015). Standard di cura della British Association of Spine Surgeons per la sindrome della cauda equina. Il giornale della colonna vertebrale, 15(3), S2-S4. https://doi.org/10.1016/j.spinee.2015.01.006
Greenhalgh, S., Finucane, L., Mercer, C., & Selfe, J. (2018). Valutazione e gestione della sindrome della cauda equina. Scienza e pratica muscoloscheletrica, 37, 69-74. https://doi.org/10.1016/j.msksp.2018.06.002
Grieve, G. P. (1994). La moderna terapia manuale di Grieve: la colonna vertebrale. 2nd Edizione. Churchill Livingstone.
Grigoryan, M., Guermazi, A., Roemer, F. W., Delmas, P. D., & Genant, H. K. (2003). Riconoscere e segnalare le fratture vertebrali osteoporotiche. Rivista europea sulla colonna vertebrale, 12(0), S104-S112. https://doi.org/10.1007/s00586-003-0613-0
Henschke, N., Maher, C. G. e Refshauge, K. M. (2007). Screening di malignità in pazienti affetti da lombalgia: una revisione sistematica. Rivista europea sulla colonna vertebrale, 16(10), 1673-1679. https://doi.org/10.1007/s00586-007-0412-0
Henschke, N., Maher, C. G., Ostelo, R. W., de Vet, H. C., Macaskill, P. e Irwig, L. (2013). Bandiere rosse per lo screening delle neoplasie nei pazienti con dolore lombare. Database Cochrane di revisioni sistematiche. https://doi.org/10.1002/14651858.cd008686.pub2
Jarvik, J. G. e Deyo, R. A. (2002). Valutazione diagnostica del dolore lombare con particolare attenzione alla diagnostica per immagini. Annali di Medicina Interna, 137(7), 586. https://doi.org/10.7326/0003-4819-137-7-200210010-00010
Lener, S., Hartmann, S., Barbagallo, G. M. V., Certo, F., Thomé, C., & Tschugg, A. (2018). Gestione delle infezioni spinali: una revisione della letteratura. Acta Neurochirurgica, 160(3), 487-496. https://doi.org/10.1007/s00701-018-3467-2
Ma, B., Wu, H., Jia, L., Yuan, W., Shi, G. e Shi, J. (2009). Sindrome della cauda equina: una revisione dei progressi clinici. 122(10), 1214-1222.
McCarthy J, Davis A. (2016). Diagnosi e gestione delle fratture da compressione vertebrale. Am Fam Physician. Jul 1;94(1):44-50. PMID: 27386723.
Nicholson, B. D., Aveyard, P., Hamilton, W., & Hobbs, F. D. R. (2019). Quando una perdita di peso inaspettata dovrebbe giustificare ulteriori indagini per escludere il cancro? BMJ, l5271. https://doi.org/10.1136/bmj.l5271
Scholz, N., (2015). Medicina personalizzata: Il trattamento giusto per la persona giusta al momento giusto EPRS | Servizio di ricerca del Parlamento europeo; Servizio di ricerca dei deputati PE 569.009
Sizer, P. S., Brismée, J.-M., & Cook, C. (2007). Screening medico per i segnali di allarme nella diagnosi e nella gestione del dolore muscoloscheletrico della colonna vertebrale. Pratica del dolore, 7(1), 53-71. https://doi.org/10.1111/j.1533-2500.2007.00112.x
Street, K. J., White, S. G., & Vandal, A. C. (2020). Prevalenza clinica e incidenza nella popolazione di patologie gravi tra i pazienti sottoposti a risonanza magnetica per la lombalgia. Il giornale della colonna vertebrale, 20(1), 101-111. https://doi.org/10.1016/j.spinee.2019.09.002
Turnpenney, J., Greenhalgh, S., Richards, L., Crabtree, A., & Selfe, J. (2013). Sviluppo di un sistema di allarme precoce per la compressione midollare metastatica (MSCC): Le carte di credito Red Flag. Ricerca e sviluppo dell'assistenza sanitaria primaria, 16(01), 14-20. https://doi.org/10.1017/s1463423613000376
Underwood, M., Buchbinder, R. (2013). Bandiere rosse per il mal di schiena. BMJ, 347: f7432.
Wilk, V. (2004). Dolore lombare acuto: valutazione e gestione. Medico di famiglia australiano, 33(6), 403-407.
Williams, C. M., Henschke, N., Maher, C. G., van Tulder, M. W., Koes, B. W., Macaskill, P., & Irwig, L. (2013). Bandiere rosse per lo screening della frattura vertebrale nei pazienti che presentano dolore lombare. Database Cochrane di revisioni sistematiche. https://doi.org/10.1002/14651858.cd008643.pub2
Yusuf, M., Finucane, L. e Selfe, J. (2019). Bandiere rosse per l'individuazione precoce di un'infezione spinale nei pazienti affetti da mal di schiena. BMC Disturbi muscoloscheletrici, 20(1). https://doi.org/10.1186/s12891-019-2949-6
Commenti
- {{ errore[0] }}