Señales de alarma en la columna vertebral
Durante demasiado tiempo, los fisioterapeutas han estado haciendo las mismas preguntas estándar para examinar médicamente a un paciente. "¿Tiene problemas de pecho o corazón, diabetes, epilepsia o problemas circulatorios?" es un ejemplo común y a menudo clínicamente irrelevante. En los últimos años, la compresión de la médula espinal ha pasado del radar de los cirujanos ortopédicos al de los fisioterapeutas y, por lo tanto, preguntas como "¿algún problema intestinal o de vejiga?" se han incluido en nuestros exámenes subjetivos. Sin embargo, esto todavía no es lo suficientemente detallado, porque, por ejemplo, un paciente puede no considerar un síntoma de patología grave como un "problema", si se ha convertido en su normalidad.
Pido disculpas por el comienzo provocador, pero en mis 34 años de experiencia clínica, he visto con demasiada frecuencia este tipo de preguntas estandarizadas.
Preguntar a un paciente sobre las señales de alarma está sujeto al razonamiento clínico, como todas nuestras preguntas. Por lo tanto, las preguntas sobre las alertas rojas deben personalizarse para cada individuo y deben perseguir el desarrollo de la hipótesis adecuada en la mente del fisioterapeuta, a partir de la información recopilada de cada paciente. Sin embargo, desarrollar una hipótesis médica adecuada puede ser nuestro primer reto, porque en medicina (y en Fisioterapia) "sólo ves lo que buscas y sólo reconoces lo que ya sabes". Esto se suele denominar "sesgo de confirmación" y se basa en que "vemos lo que queremos ver", porque sólo así podemos creer que podemos ayudar al paciente (necesitamos saber qué estamos tratando para saber cómo tratarlo). Por eso es importante ampliar al máximo nuestros conocimientos médicos, ¡para evitar que se nos escape algo que desconocemos!
Esto se aplica incluso a algunos de los diagnósticos más obvios, por no hablar de los diagnósticos más complejos y raros. Por ejemplo, hasta 70% de las fracturas vertebrales se diagnostican erróneamente y hasta 75% de las infecciones vertebrales se diagnostican inicialmente de forma incorrecta (Grigoryan et al 2003, McCarthy & Davis 2016). La infección medular es difícil de reconocer clínicamente. En los pacientes que he visto con infección espinal, sabía que había algo muy mal con el paciente, pero no sabía exactamente qué, y sólo las investigaciones apropiadas descubrieron el diagnóstico. Así que esto también forma parte de nuestro papel en el cribado: tenemos que saber cuándo son necesarias más investigaciones y qué investigaciones pueden ser útiles.
Si consideramos la diferencia entre el diagnóstico Médico y un diagnóstico Fisioterapéutico, el primero trata de encontrar la causa del problema del paciente y como Fisio tratamos las consecuencias del problema. Determinar las consecuencias se basa principalmente en los hallazgos clínicos, sin embargo determinar la causa del sufrimiento de un paciente se basa en gran medida en el conocimiento teórico y por lo tanto se encuentra en el ámbito del Modelo Biomédico. Por lo tanto, como fisioterapeutas deberíamos trabajar principalmente en el modelo biopsicosocial, pero aún así debemos tener en cuenta el modelo biomédico en nuestra función de exploración médica.
En pocas palabras, el enfoque biomédico puede utilizarse para detectar señales de alarma en el paciente y afecciones que requieren atención médica precoz y, a continuación, debe considerarse el enfoque biopsicosocial para comprender cómo está afectando el problema al paciente, centrándose en los signos y síntomas más que en el diagnóstico estructural. Como puede verse en el diagrama siguiente, la detección de banderas rojas debe ser un componente prioritario en el proceso de exploración, en todos nuestros pacientes.
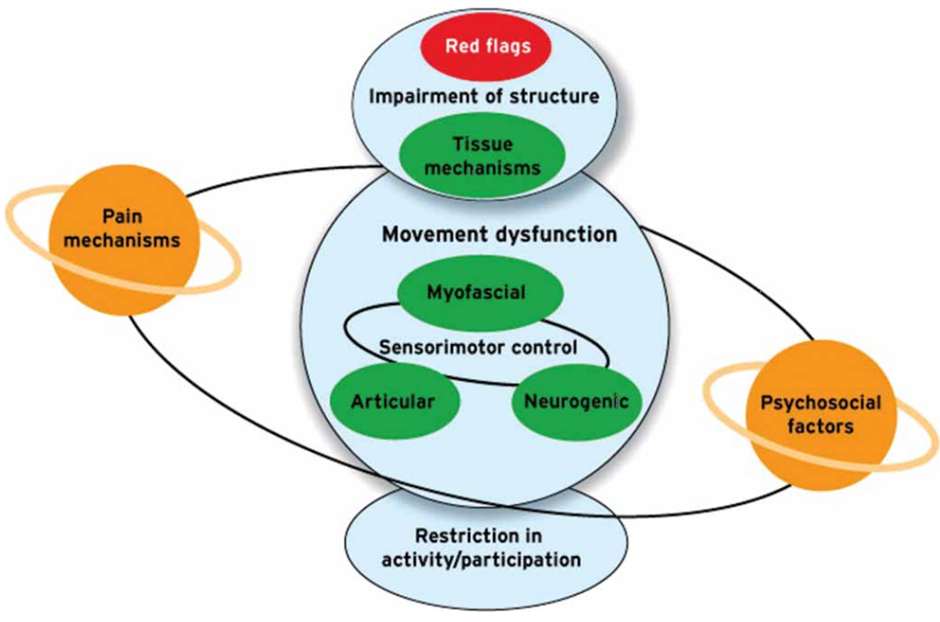
Hay que reconocer nuestra dificultad para establecer un diagnóstico médico de los pacientes con dolor lumbar, por ejemplo, pero, a pesar de ello, el modelo biomédico sigue teniendo un papel que desempeñar a la hora de orientar las decisiones relacionadas con el tratamiento, el cribado médico y el pronóstico de los pacientes. Al considerar el diagnóstico médico, el paciente está siendo clasificado médicamente y, por lo general, esto se puede hacer a través de una historia detallada apoyada por exámenes médicos (análisis de sangre, escáneres, etc.) en lugar de basarse en los resultados de las pruebas físicas.
Es imprudente suponer que si su paciente ha visitado a un médico antes de su cita, es que ya ha sido examinado médicamente. Los médicos suelen tener un tiempo muy limitado con sus pacientes y tengo muchos ejemplos de pacientes con patologías graves que ya han visto a su médico de cabecera. Además, como fisioterapeutas pensamos de forma muy musculoesquelética y, como resultado, es tentador creer que todos los pacientes que vemos tienen un problema musculoesquelético. Por lo tanto, tanto si se trabaja como médico de primer contacto (en el sector público en algunos países y/o en el sector privado en la mayoría de los países) o como médico secundario, es necesario realizar un cribado de bandera roja basado en conocimientos médicos para asegurarse de que no se está tratando a un paciente que debería ser tratado en otro lugar. "Acudir a la persona adecuada, en el momento adecuado, para recibir el tratamiento adecuado" (Boletín informativo sobre salud del Parlamento Europeo 2015).
Las banderas rojas son posibles indicadores de patología grave, señales de advertencia de que la Fisioterapia puede no o guías de predicción clínica. Deben constituir un motivo claro para seguir investigando o remitir al paciente a un médico.

Al fin y al cabo, a nadie le interesa tratar a un lobo con piel de cordero.
Las directrices clínicas para el tratamiento fisioterapéutico del dolor lumbar persistente (CSP, 2007) indican que hay 163 elementos individuales que podrían considerarse señales de alarma de patología espinal, 119 en la historia clínica subjetiva y 44 en la exploración física. Claramente esto representa un problema en la utilidad clínica práctica de las banderas rojas. Además, se carece de pruebas sólidas que respalden el carácter informativo de la mayoría de las señales de alarma. Henschke et al (2013) han informado de que las banderas rojas combinadas son prometedoras, pero se necesitan más estudios de validación.
Sin embargo, las señales de alarma siguen considerándose el indicador clínico más fiable de una posible patología grave y siguen siendo fundamentales en nuestro proceso de evaluación (Underwood, 2013). Dado que la gravedad de determinadas señales de alarma justifica una actuación inmediata y que otras solo justifican una observación conservadora, es importante clasificar cada hallazgo y responder en función del nivel de gravedad que presente. Algunas banderas son más rojas que otras.
Sizer et al (2007) clasificaron las banderas rojas en 3 grupos:
- Categoría I
- Factores que requieren atención médica inmediata
- Categoría II
- Factores que requieren un interrogatorio subjetivo y procedimientos cautelares de examen y tratamiento
- Categoría III
- Factores que requieren más pruebas físicas y análisis de diferenciación
Cualquier señal de alarma de la categoría I puede sugerir una patología grave. Estas incluyen déficit neurológico no explicado por una mono-radiculopatía, cambios sensoriales en la región perianal, cambios patológicos en el intestino y la vejiga, patrón no mecánico de los síntomas, déficit neurológico progresivo y masas abdominales pulsátiles.
Las señales de alarma de categoría II incluyen edad de inicio > 50 años, clonus, fiebre, elevación de los análisis de sangre inflamatorios (VSG), déficit de la marcha, antecedentes de un trastorno con predilección de infección o hemorragia, o un trastorno óseo metabólico, o cáncer, uso prolongado de corticosteroides, llagas o heridas que no cicatrizan y antecedentes recientes de pérdida de peso inexplicable.
Una sola bandera roja de categoría II puede no ser motivo de preocupación, pero cuantas más banderas rojas identifique en un paciente, más debe aumentar su índice de sospecha. También hay que tener en cuenta ciertos grupos de señales de alarma; un paciente con dolor lumbar de más de 50 años de edad y que toma esteroides a largo plazo tiene muchas más probabilidades de sufrir una fractura por compresión vertebral. Según Jarvik et al (2002), un paciente en el que haya fracasado el tratamiento conservador previo + pérdida de peso inexplicable + antecedentes de cáncer + edad superior a 50 años = una sensibilidad de casi 100% para identificar un tumor maligno.
Las señales de alarma de categoría III incluyen reflejos anormales, radiculopatía o parestesia bilateral o unilateral, dolor referido inexplicable y debilidad significativa inexplicable de las extremidades superiores o inferiores.
Además, existen señales de alarma inespecíficas, como una presentación clínica que difiere de los patrones clínicos conocidos, la ausencia de respuesta al tratamiento (mejor o peor) y un comportamiento de los síntomas a lo largo del tiempo que no coincide con el pronóstico. Cualquiera de estas manifestaciones clínicas debe hacer pensar en una posible afección no mecánica, que puede requerir más investigaciones y/o intervenciones médicas.
En cuanto a las etiologías graves de la columna vertebral, las 4 más comunes a tener en cuenta son el síndrome de cauda equina, la fractura, las lesiones benignas o malignas y la infección. El reconocimiento precoz de una patología grave depende más de la concienciación, la vigilancia y la sospecha que de las normas (Grieve, 1994). La concienciación procede del aumento de nuestros conocimientos médicos y la vigilancia está relacionada con el detalle con que interrogamos y examinamos a cada paciente. Como la mayoría de las señales de alarma se encuentran en el examen subjetivo, es esencial que estemos atentos al interrogatorio de cada paciente.
Síndrome de Cauda Equina (CES):

Lamentablemente, no existen criterios diagnósticos definitivos ampliamente aceptados para la CES. Fraser et al (2009) identificaron 17 definiciones diferentes. Nuestro reto diagnóstico se ve agravado por el hecho de que los signos y síntomas iniciales suelen ser sutiles y vagos, y varían en intensidad y progresión. Sólo mediante una anamnesis y una exploración cuidadosas y detalladas del paciente se puede diagnosticar precozmente la CES y, por tanto, tratarla a tiempo para evitar una discapacidad de por vida (Ma et al, 2009).
De todas las banderas rojas enumeradas en relación con CES hay existen 5 características clave que se describen de forma consistente en la literatura y que, por lo tanto, deben constituir la base de sus preguntas relacionadas con el diagnóstico. Se trata de ciática bilateral neurogénica, disminución de la sensibilidad perineal, retención indolora de la vejiga, pérdida del tono anal y pérdida de la función sexual. El nivel de evidencia de todos estos signos y síntomas por sí solos es BAJO. Así que, de nuevo, hay que confiar en el juicio clínico y considerar el cuadro en su conjunto, y cuantos más hallazgos significativos se produzcan, más debe aumentar el índice de sospecha. La historia y la cronología son importantes. Si todos los cambios son recientes, puede ser necesaria una derivación urgente.
Greenhalgh et al en 2018, aconsejaron un poco más de detalle a nuestro interrogatorio de intestino y vejiga para ayudar a la detección de CES. Aconsejaron 3 preguntas de cribado importantes:
Pregunta vital 1: ¿Ha notado entumecimiento o sensaciones extrañas alrededor de las nalgas o entre las piernas? ¿Siente el papel higiénico normal cuando se limpia las nalgas?
Pregunta vital 2: ¿Tu vejiga funciona con normalidad? ¿Sabe cuándo está llena? ¿Ha tenido pérdidas de control (accidentes) o dificultades para orinar? ¿O ha tenido ganas de orinar todo el tiempo?
Pregunta vital 3: ¿Ha experimentado algún problema inusual con sus intestinos recientemente? ¿Ha notado algún cambio en la función sexual, como pérdida de sensibilidad en los genitales o incapacidad para tener una erección o eyacular?
Si se sospecha una EEC, toda la bibliografía coincide en la necesidad de una opinión médica y una intervención urgentes, por lo que es apropiado remitir al paciente al servicio de urgencias. La descompresión quirúrgica precoz es esencial, lo que cuenta con una gran cantidad de bibliografía de apoyo, pero hay discrepancias en cuanto al momento: muchos autores afirman que la cirugía es óptima en un plazo de 48 horas (desde el inicio de la disfunción intestinal o urinaria) para una buena recuperación. Por lo tanto, aunque el diagnóstico precoz es difícil, si tiene alguna sospecha, es mejor prevenir que curar y derivar cuanto antes. "No se gana nada retrasando la cirugía y se puede perder mucho" (Germon et al, 2015).
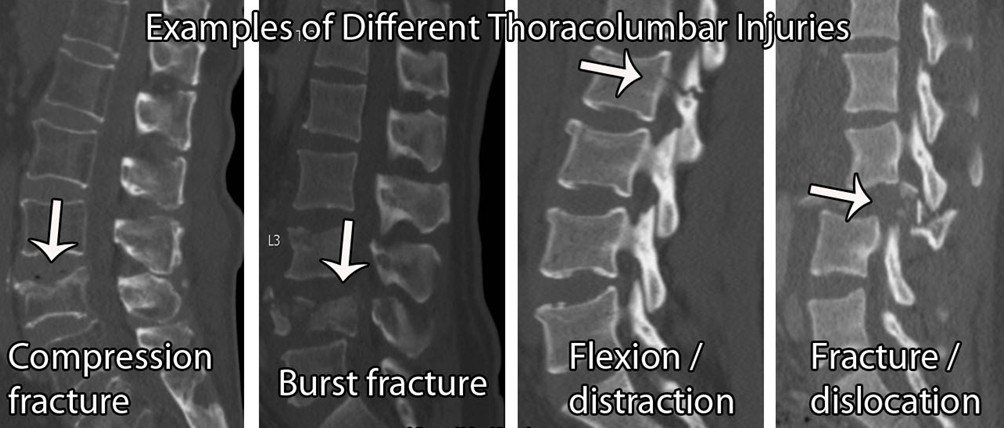
Fractura vertebral:
En general, las banderas rojas para el diagnóstico de fracturas vertebrales son poco útiles. Hay muchos falsos positivos, con una precisión diagnóstica baja (Williams et al 2013). Por lo tanto, si se sospecha una fractura, es importante interrogar al paciente sobre los factores de riesgo más generales.
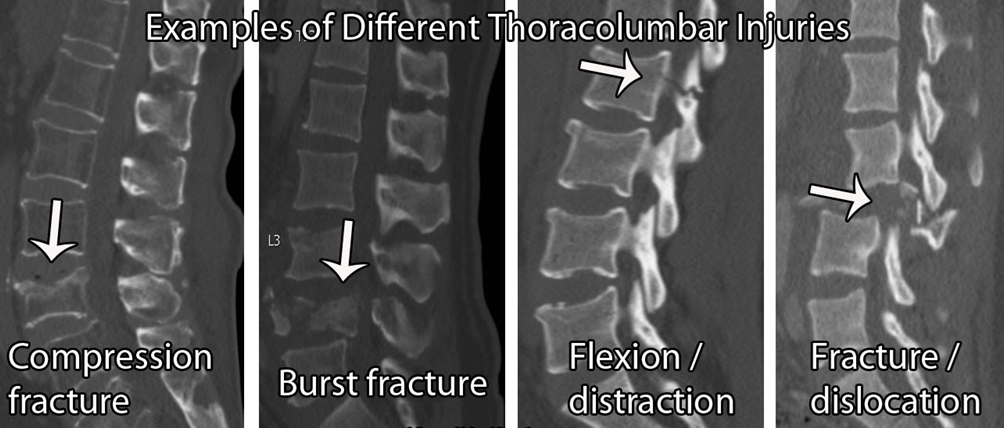
Los factores de riesgo para el debilitamiento óseo incluyen; exceso de alcohol (≥ 3 unidades al día), deficiencia de vitamina D, uso prolongado de esteroides (≥5mg/día durante 3 meses), artritis reumatoide, diabetes, tabaquismo ( ≥ 20/día), restricciones dietéticas, trastornos de la alimentación, problemas de absorción, por ejemplo, enfermedad de Crohn. Ahora bien, de nuevo, el nivel de evidencia de la mayoría de ellos por sí solos es bajo y, por lo tanto, cuantos más resultados positivos se obtengan, más sospechosos serán.
Si un paciente acude a su consulta con un dolor torácico o lumbar de aparición súbita, en su lista de sospechosos debe figurar una fractura. Esta hipótesis se confirmaría aún más si el paciente tiene antecedentes de fracturas osteoporóticas previas, otros factores de riesgo osteoporótico (como los mencionados anteriormente), antecedentes de cáncer, osteoporosis o mieloma conocidos, sensibilidad ósea en la línea media y/o una edad de inicio superior a 65 años en las mujeres o superior a 75 años en los hombres.
Tumor maligno espinal:
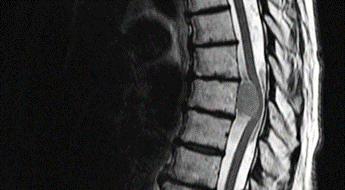
Después de la fractura vertebral, la enfermedad ósea metastásica es la 2nd afección grave más frecuente de la columna vertebral. Las metástasis óseas espinales son frecuentes en los cánceres de mama, bronquios/pulmón, tiroides, riñones y próstata. Una vez más, la mala noticia es que no existen señales de alarma específicas para los tumores malignos de la columna vertebral, por lo que debemos tener en cuenta las señales de alarma del cáncer en general.
Entre ellas figuran:
Dolor con alivio mínimo (constante/constante y por la noche), pero tenga en cuenta que algunos dolores del cáncer se alivian con medicamentos y que el dolor no siempre es una presentación temprana,
Antecedentes de cáncer,
Una edad de inicio > 50 años, o menos de 20 años
Fatiga, malestar sistémico,
Pérdida de peso (hasta 5-10% del peso corporal durante 3-6 meses, Nicholson et al 2019), pero tenga en cuenta que la pérdida de peso no siempre es un factor, especialmente en las primeras etapas.
En una revisión sistemática realizada por Henschke et al en 2007, se halló que las características y pruebas más útiles para el cribado de neoplasias malignas en pacientes con dolor lumbar son los antecedentes de cáncer, la elevación de la VSG, la reducción del hematocrito y el juicio clínico. El único factor con un alto nivel de evidencia es la historia previa de cánceres con predilección por la metástasis.
La presencia de metástasis en la columna vertebral podría evolucionar a una compresión medular metastásica (CMM). De las 163 señales de alarma, ninguna es específica de la CMM. El reto para nosotros es que es difícil de diagnosticar, y el diagnóstico precoz es muy importante porque, los retrasos en el diagnóstico y el tratamiento pueden provocar paraplejia y doble incontinencia.
Turnpenney et al. (2013) elaboraron una lista de signos de alerta temprana de MSCC, que debemos considerar como base para nuestro cuestionamiento de bandera roja:
Rl dolor de espalda multisegmentario o en banda,
EDolor escalar, mala respuesta al tratamiento,
Dcarácter o localización diferente a los síntomas anteriores,
Fsensaciones extrañas o piernas pesadas,
Lying plana aumenta el dolor de espalda,
Adolor gonizante que causa angustia y desesperación,
GTrastorno del apetito, inestabilidad, especialmente en las escaleras,
SLepra muy alterada con dolor peor por la noche.
Cualquier combinación de estas banderas rojas debería aumentar sus sospechas y cuantas más banderas rojas, mayor será el riesgo y mayor la urgencia de derivar al paciente para que reciba ayuda médica.
Infección espinal:

La infección espinal se refiere a cualquier enfermedad infecciosa de las estructuras espinales, por ejemplo, las vértebras, los discos o los tejidos paraespinales adyacentes. Una vez más, por desgracia, la infección de la columna vertebral es difícil de reconocer clínicamente. En los países de renta alta y media-alta, la tasa de infección ha aumentado de forma constante, posiblemente debido al creciente envejecimiento de la población y al aumento del consumo de drogas por vía intravenosa. En los países de renta baja también ha aumentado, quizá debido a las epidemias de VIH/sida y tuberculosis (TB) (Lener et al, 2018).
Al considerar una infección medular, de nuevo es importante interrogar adecuadamente al paciente, lo que implicaría la detección de los factores de riesgo asociados (Yusuf et al, 2019).
Entre ellas figuran:
Comorbilidades inmunosupresoras como diabetes, uso prolongado de esteroides, tabaquismo, VIH/SIDA;
Factores sociales como el consumo de drogas intravenosas, la obesidad y los antecedentes familiares de tuberculosis;
Factores ambientales como las condiciones de vida (hacinamiento, falta de vivienda, encarcelamiento) y el país de nacimiento (nacido en un país donde la tuberculosis es endémica);
Cirugía espinal previa.
Todas las pruebas de las banderas rojas que indican infección espinal individualmente, son de un nivel bajo. Así que, de nuevo, cuantas más señales de alarma se encuentren, más debe elevarse el nivel de sospecha, y hay que confiar hasta cierto punto en el juicio clínico. Las cuestiones que deben plantearse y analizarse en el examen subjetivo son la constancia del dolor (C/C), el dolor de alta intensidad, la aparición súbita, la fiebre, los escalofríos, la sudoración, la erupción cutánea (Herpes zoster), la fatiga, el malestar general, la pérdida de peso inexplicable, la cirugía o infección reciente (últimas 4 semanas) y el dolor nocturno (>60 minutos para establecerse).
El tiempo que transcurre entre el inicio de una infección y el diagnóstico suele ser prolongado. Los pacientes pueden estar relativamente sanos hasta que los síntomas se manifiestan en las últimas fases. La progresión suele ser más lineal (la progresión de la malignidad puede tener altibajos). De la tríada infecciosa (dolor vertebral, fiebre y disfunción neurológica), el dolor lumbar es el síntoma más frecuente, que puede evolucionar a síntomas neurológicos. Sin embargo, muchas personas no presentan los 3, solo 50% de los pacientes informan fiebre (Lener et al 2018). Por lo tanto, la ausencia de fiebre no puede descartar una infección espinal. La progresión no tratada puede conducir a parálisis, inestabilidad espinal y fatalidad. Por lo tanto, al igual que con todas estas afecciones, vale la pena señalar que no derivar a un paciente según sea necesario, es una forma de hacer daño al paciente, que es algo que nuestro cribado de banderas rojas está tratando de evitar.
Conclusión:
La prevalencia de patologías graves de la columna vertebral es rara, y la bibliografía cita desde 1% (Wilk, 2004) hasta 14,8% (Street et al, 2020). Sin embargo, podemos ver rápidamente a 100 pacientes con dolor lumbar y algunos de ellos podrían tener una causa siniestra y necesitar estar en otro lugar que no sea su clínica. Por lo tanto, los clínicos deben ser capaces de identificar a los pacientes que requerirán intervención médica y nuestra mejor oportunidad de conseguirlo es con un interrogatorio apropiado, clínicamente razonado y detallado.
Buena suerte y mis mejores deseos,
Matthew

Referencias:
Finucane, L. M., Downie, A., Mercer, C., Greenhalgh, S. M., Boissonnault, W. G., Pool-Goudzwaard, A. L., Beneciuk, J. M., Leech, R. L., & Selfe, J. (2020). Marco Internacional de Banderas Rojas para Potenciales Patologías Graves de la Columna Vertebral. Revista de fisioterapia ortopédica y deportiva, 50(7), 1-23. https://doi.org/10.2519/jospt.2020.9971
Fraser, S., Roberts, L., & Murphy, E. (2009). Cauda Equina Syndrome: A Literature Review of Its Definition and Clinical Presentation. Archivos de Medicina Física y Rehabilitación, 90(11), 1964-1968. https://doi.org/10.1016/j.apmr.2009.03.021
Germon, T., Ahuja, S., Casey, A. T. H., Todd, N. V., & Rai, A. (2015). British Association of Spine Surgeons standards of care for cauda equina syndrome. Revista de la columna vertebral, 15(3), S2-S4. https://doi.org/10.1016/j.spinee.2015.01.006
Greenhalgh, S., Finucane, L., Mercer, C., & Selfe, J. (2018). Evaluación y manejo del síndrome de cauda equina. Ciencia y práctica musculoesquelética, 37, 69-74. https://doi.org/10.1016/j.msksp.2018.06.002
Grieve, G. P. (1994). Terapia manual moderna de Grieve : la columna vertebral. 2nd Edición. Churchill Livingstone.
Grigoryan, M., Guermazi, A., Roemer, F. W., Delmas, P. D., & Genant, H. K. (2003). Recognizing and reporting osteoporotic vertebral fractures. Revista Europea de la Columna Vertebral, 12(0), S104-S112. https://doi.org/10.1007/s00586-003-0613-0
Henschke, N., Maher, C. G., & Refshauge, K. M. (2007). Screening for malignancy in low back pain patients: a systematic review. Revista Europea de la Columna Vertebral, 16(10), 1673-1679. https://doi.org/10.1007/s00586-007-0412-0
Henschke, N., Maher, C. G., Ostelo, R. W., de Vet, H. C., Macaskill, P., & Irwig, L. (2013). Red flags to screen for malignancy in patients with low-back pain. Base de datos Cochrane de revisiones sistemáticas. https://doi.org/10.1002/14651858.cd008686.pub2
Jarvik, J. G., y Deyo, R. A. (2002). Evaluación diagnóstica del dolor lumbar con énfasis en el diagnóstico por imagen. Anales de Medicina Interna, 137(7), 586. https://doi.org/10.7326/0003-4819-137-7-200210010-00010
Lener, S., Hartmann, S., Barbagallo, G. M. V., Certo, F., Thomé, C., & Tschugg, A. (2018). Manejo de la infección espinal: una revisión de la literatura. Acta Neurochirurgica, 160(3), 487-496. https://doi.org/10.1007/s00701-018-3467-2
Ma, B., Wu, H., Jia, L., Yuan, W., Shi, G., & Shi, J. (2009). Síndrome de cauda equina: revisión del progreso clínico. 122(10), 1214-1222.
McCarthy J, Davis A. (2016). Diagnóstico y manejo de las fracturas por compresión vertebral. Am Fam Physician. Jul 1;94(1):44-50. PMID: 27386723.
Nicholson, B. D., Aveyard, P., Hamilton, W., & Hobbs, F. D. R. (2019). Cuándo una pérdida de peso inesperada debe justificar una investigación adicional para excluir el cáncer? BMJ, l5271. https://doi.org/10.1136/bmj.l5271
Scholz, N., (2015). Medicina personalizada: El tratamiento adecuado para la persona adecuada en el momento adecuado EPRS | Servicio de Investigación del Parlamento Europeo; Servicio de Investigación de los Diputados PE 569.009
Sizer, P. S., Brismée, J.-M., & Cook, C. (2007). Medical Screening for Red Flags in the Diagnosis and Management of Musculoskeletal Spine Pain. Práctica del dolor, 7(1), 53-71. https://doi.org/10.1111/j.1533-2500.2007.00112.x
Street, K. J., White, S. G., & Vandal, A. C. (2020). Clinical prevalence and population incidence of serious pathologies among patients undergoing magnetic resonance imaging for low back pain. Revista de la columna vertebral, 20(1), 101-111. https://doi.org/10.1016/j.spinee.2019.09.002
Turnpenney, J., Greenhalgh, S., Richards, L., Crabtree, A., & Selfe, J. (2013). Desarrollo de un sistema de alerta temprana para la compresión medular metastásica (CMM): Tarjetas de crédito de bandera roja. Investigación y Desarrollo en Atención Primaria, 16(01), 14-20. https://doi.org/10.1017/s1463423613000376
Underwood, M., Buchbinder, R. (2013). Banderas rojas para el dolor de espalda. BMJ, 347: f7432.
Wilk, V. (2004). Lumbalgia aguda: evaluación y tratamiento. Médico de familia australiano, 33(6), 403-407.
Williams, C. M., Henschke, N., Maher, C. G., van Tulder, M. W., Koes, B. W., Macaskill, P., & Irwig, L. (2013). Red flags to screen for vertebral fracture in patients presenting with low-back pain. Base de datos Cochrane de revisiones sistemáticas. https://doi.org/10.1002/14651858.cd008643.pub2
Yusuf, M., Finucane, L., & Selfe, J. (2019). Banderas rojas para la detección temprana de la infección espinal en pacientes con dolor de espalda. BMC Trastornos musculoesqueléticos, 20(1). https://doi.org/10.1186/s12891-019-2949-6
Comentarios
- {{ error[0] }}